Nồng độ phần trăm cho biết số gam chất tan có
I. Nồng độ phần trăm: (C%)
* Nồng độ phần trăm (kí hiệu C%) của dung dịch cho biết số gam chất tan có trong 100 gam dung dịch.
Công thức: $C\%=\frac{{{m}_{ct}}}{{{m}_{dd}}}.100\%$
Trong đó : C% : nồng độ phần trăm của dung dịch (%)
mct : khối lượng chất tan (gam)
mdd : khối lượng dung dịch (gam) = mdung môi + mchất tan
Từ công thức tính nồng độ phần trăm, ta suy ra các công thức sau:
- Công thức tính khối lượng dung dịch: ${{m}_{dd}}=\frac{{{m}_{ct}}.100\%}{C\%}$
- Công thức tính khối lượng chất tan: ${{m}_{ct}}=\frac{{{m}_{dd}}.C\%}{100\%}$
Ví dụ 1: Hoà tan 10 gam đường vào 40 gam nước. Tính nồng độ phần trăm của dung dịch thu được.
Giải:
Khối lượng chất tan là: mct = 10 gam
Khối lượng dung dịch thu được là: mdd = mdm + mct = 40 + 10 = 50 gam
Áp dụng công thức: $C\%=\frac{{{m}_{ct}}}{{{m}_{dd}}}.100\%=\frac{10}{50}.100\%=20\%$
II. Nồng độ mol của dung dịch (CM)
* Nồng độ mol (kí hiệu CM) của dung dịch cho biết số mol chất tan có trong một lít dung dịch.
Công thức tính: ${{C}_{M}}=\frac{n}{{{V}_{dd}}}$
Trong đó: CM là nồng độ mol (mol/lit)
n là số mol chất tan (mol)
Vdd là thể tích dung dịch (lit)
- Các công thức được suy ra từ công thức tính nồng độ mol của dung dịch:
+ Công thức tính số mol chất tan: n = CM . V
+ Công thức tính thể tích dung dịch: ${{V}_{dd}}=\frac{n}{{{C}_{M}}}$
Ví dụ: Tính khối lượng H2SO4 có trong 50 ml dung dịch H2SO4 2M
Giải:
Số mol H2SO4 có trong dung dịch H2SO4 2M là: ${{n}_{{{H}_{2}}S{{O}_{4}}}}$ = CM . V = 2 . 0,05 = 0,1 mol
=> Khối lượng H2SO4 là: ${{m}_{{{H}_{2}}S{{O}_{4}}}}$ = n . M = 0,1.98 = 9,8 gam
* Công thức chuyển đổi giữa nồng độ phần trăm và nồng độ mol:
Công thức tính nồng độ phần trăm: $C\%=\frac{{{m}_{ct}}}{{{m}_{dd}}}.100\%$ (1)
Khối lượng dung dịch được tính theo công thức: mdd = Ddd . V
với Ddd là khối lượng riêng của dung dịch (gam/lít) ; V là thể tích của dung dịch (lít)
Khối lượng chất tan là: mct = n . M
Thay vào (1) ta có: $C\%=\frac{n.M}{{{D}_{dd}}.V}.100\%=\frac{n}{V}.\frac{M}{{{D}_{dd}}}.100\%$
Mà ${{C}_{M}}=\frac{n}{V}$ => $C\%=\frac{{{C}_{M}}.M}{{{D}_{dd}}}.100\%$
=> Công thức chuyển từ nồng độ phần trăm sang nồng độ mol: ${{C}_{M}}=\frac{C\%.{{D}_{dd}}}{M.100\%}$
Lưu ý: Công thức tính này lấy đơn vị của Ddd là gam/lít, thường các đầu bài cho đơn vị của Ddd là gam/ml nên ta cần đổi lại đơn vị để áp dụng công thức.
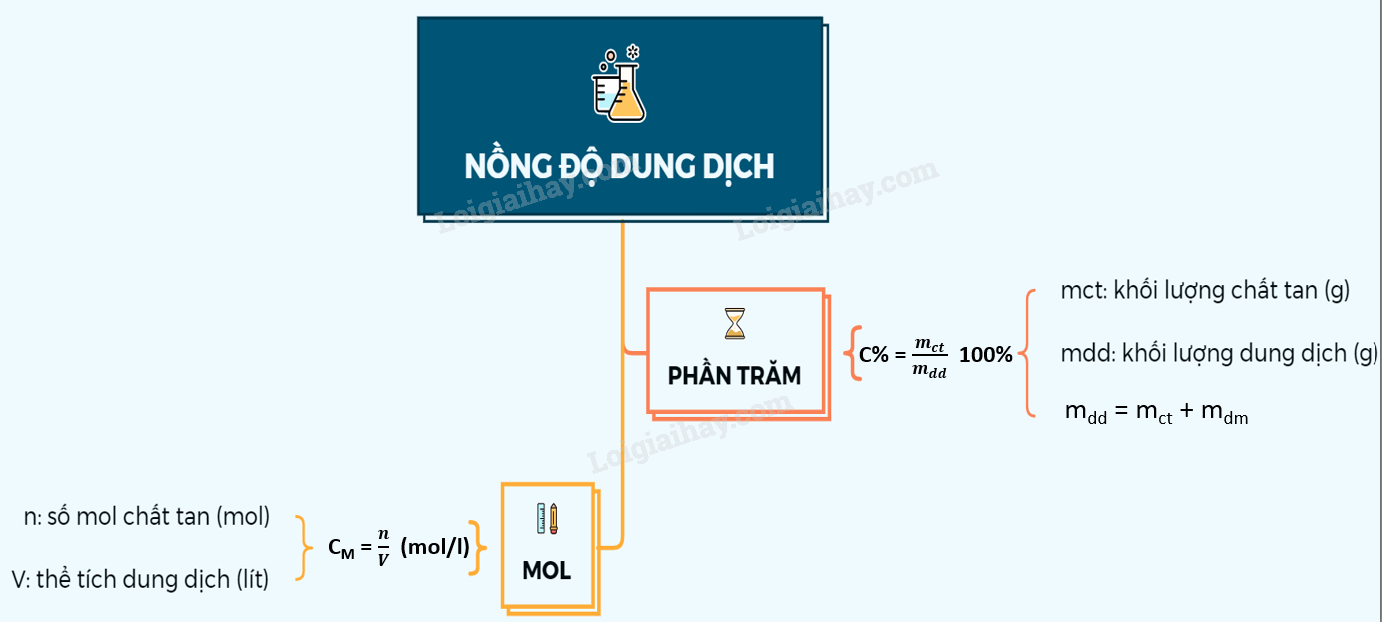
Sơ đồ tư duy: Nồng độ dung dịch
Bình luận
![]() Chia sẻ
Chia sẻ
-
Bài 1 trang 145 SGK Hóa học 8
Bằng cách nào có được 200 g
-
Bài 2 trang 145 SGK Hóa học 8
Tìm nồng độ mol của 850 ml
-
Bài 3 trang 146 SGK Hóa học 8
Hãy tính nồng độ mol của mỗi dung dịch sau:
-
Bài 4 trang 146 SGK Hóa học 8
Hãy tính số mol và số gam chất tan
-
Bài 5 trang 146 SGK Hóa học 8
Giải bài 5 trang 146 SGK Hóa học 8. Hãy tính nồng độ phần trăm của những dung dịch sau:
>> Xem thêm
Luyện Bài Tập Trắc nghiệm Hóa lớp 8 - Xem ngay
Tham Gia Group Dành Cho 2K10 Chia Sẻ, Trao Đổi Tài Liệu Miễn Phí

>> Học trực tuyến lớp 8 trên Tuyensinh247.com cam kết giúp học sinh lớp 8 học tốt, hoàn trả học phí nếu học không hiệu quả.










